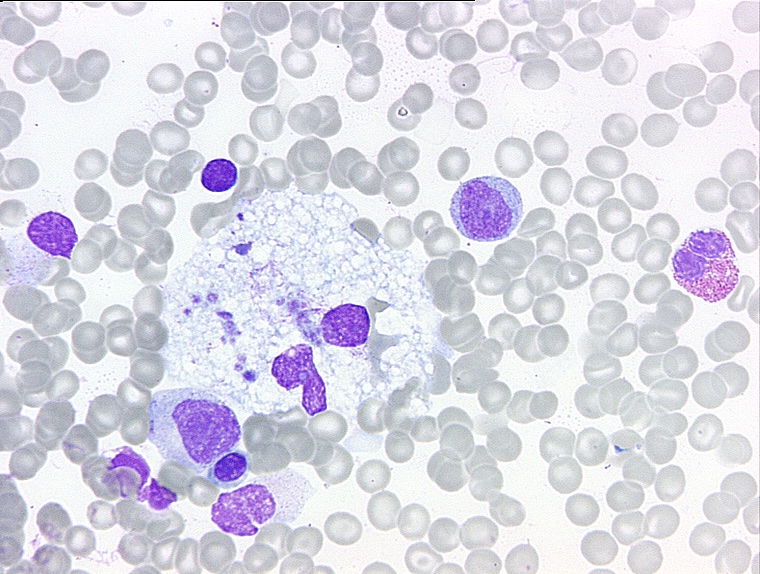
Was sind Lysomale Speichererkankungen?
Lysosomale Speicherkrankheiten (Lysosomal Storage Disorders, LSD) sind eine Gruppe von mehr als 50 seltenen erblichen Stoffwechselkrankheiten. Die Krankheiten sind gekennzeichnet durch eine abnorme Anhäufung verschiedener toxischer Stoffe in den Körperzellen als Folge von Enzymmängeln.
Lysosomale Speicherkrankheiten betreffen das Lysosom, eine Struktur in den Zellen, die Stoffe wie Proteine, Kohlenhydrate und alte Zellteile abbaut, damit der Körper sie wiederverwerten kann. Infolgedessen können verschiedene Teile des Körpers betroffen sein, darunter das Skelett, das Gehirn, die Haut, das Herz und das zentrale Nervensystem. Neue lysosomale Speicherkrankheiten werden weiterhin identifiziert.